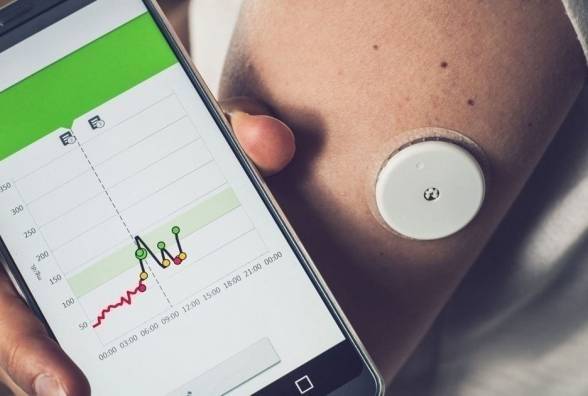
Новый способ активации инсулин-продуцирующих клеток! Исследование
Исследователи из Университета Тафтса трансплантировали сконструированные бета-клетки поджелудочной железы мышам с диабетом, а затем заставили клетки вырабатывать инсулин более чем в два-три раза выше обычного уровня, подвергая их воздействию света. “Переключаемые” светом клетки предназначены для компенсации снижения выработки инсулина или снижения инсулиновой реакции у людей с диабетом. Исследование, опубликованное в ACS Synthetic Biology, показывает, что уровни глюкозы можно контролировать на мышиной модели с диабетом без фармакологического вмешательства.
- Автор: Людмила Панчук, редакторка
- access_time
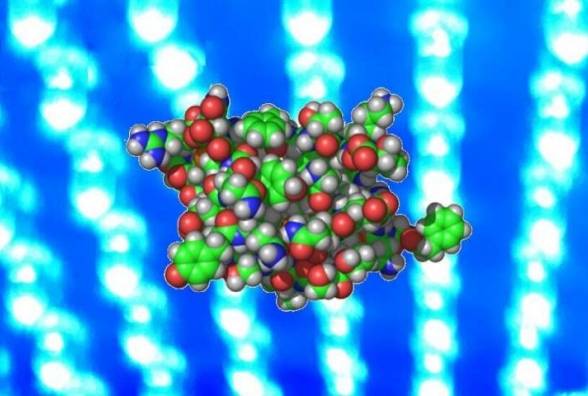
Исследователи стремились разработать новый способ усиления выработки инсулина, сохраняя при этом важную связь между высвобождением инсулина и концентрацией глюкозы в крови в режиме реального времени. Они достигли этого, используя преимущества «оптогенетики», подхода, основанного на белках, которые изменяют свою активность под влиянием светового сигнала. Бета-клетки поджелудочной железы были созданы с геном, который кодирует фотоактивируемый фермент аденилатциклазу (PAC). PAC вырабатывает молекулу циклического аденозинмонофосфата (cAMP) при воздействии синего света, который, в свою очередь, запускает стимулируемую глюкозой выработку инсулина в бета-клетке.
Так, производство инсулина может увеличиться в два-три раза, но только при высоком уровне глюкозы в крови. При низких уровнях глюкозы выработка инсулина остается низкой. Это позволяет избежать случаев гипогликемии - главного недостатка в процессе компенсации диабета.
Исследователи обнаружили, что пересадка сконструированных бета-клеток поджелудочной железы под кожу мышей с диабетом приводила к улучшению толерантности и регуляции уровня глюкозы, снижению гипергликемии и повышению уровня инсулина в плазме при воздействии освещения синим светом.
«Это обратная аналогия, но мы на самом деле используем свет для включения и выключения биологического переключателя», - сказал Эммануэль Цанакакис, профессор химической и биологической инженерии в Школе инженерии в Университете Тафтса и автор исследования. «Таким образом, мы можем помочь в диабетическом контексте лучше контролировать и поддерживать надлежащие уровни глюкозы без фармакологического вмешательства. Клетки выполняют работу по производству инсулина естественным образом, и регуляторные контуры в них работают одинаково; мы просто увеличиваем количество молекул cAMP в бета-клетках, чтобы заставить их вырабатывать больше инсулина только тогда, когда это необходимо ".
Синий свет просто меняет переключатель из нормального режима в режим усиления. Такие оптогенетические подходы, использующие активируемые светом белки для модуляции функции клеток, изучаются во многих биологических системах и стимулируют усилия по разработке принципиально нового вида лечения.
«Есть несколько преимуществ использования такого подхода, как управление светом», - сказал Фан Чжан, аспирант лаборатории Цанакакиса в Тафтсе и первый автор исследования. «Очевидно, что ответ на сигналы является моментальным; и, несмотря на увеличивающуюся секрецию инсулина, количество кислорода, потребляемое клетками, существенно не меняется, как показывает наше исследование. Кислородное голодание является распространенной проблемой в исследованиях с участием трансплантированных клеток поджелудочной железы».
Цікаві рецепти пасок для людей з діабетом
Вітаміни та БАДи, які потенційно корисні при діабеті
Капуста при діабеті: поживні властивості та користь для здоров'я
10 порад, щоб залишатися в цільовому діапазоні глюкози при діабеті 1 типу
«Тихий вбивця»: чим небезпечний високий рівень тригліцеридів при діабеті, та як його знизити
Гіпонеусвідомленість: 5 способів захистити себе, якщо ви не відчуваєте симптомів низького цукру
Лікування діабету за допомогою пробіотиків та синбіотиків. Що показало нове дослідження?
4 найгірші продукти для сніданку, якщо у вас діабет або переддіабет
Електронні сигарети та вейпи — чи безпечні вони для людей з діабетом?
Автономна нейропатія шлунку та її вплив на компенсацію діабету

Моя Цукрова Школа від 14 лютого 2024
Читати номер













Ви не авторизовані